進口醫療器械與醫護人員防護用品注冊備案全流程詳解

隨著我國醫療市場的不斷開放和醫療服務水平的提升,越來越多的進口醫療器械和醫護人員防護用品進入中國市場。為確保這些產品在中國境內使用的安全性和有效性,并符合國家相關法律法規要求,所有進口醫療器械和特定的醫護人員防護用品(通常屬于醫療器械范疇)都必須經過國家藥品監督管理局(NMPA,原CFDA)的注冊或備案流程。本文將為您詳細解讀這一關鍵流程。
一、 核心概念界定與監管分類
需要明確兩個核心概念:
- 醫療器械:根據《醫療器械監督管理條例》,是指直接或者間接用于人體的儀器、設備、器具、體外診斷試劑及校準物、材料以及其他類似或者相關的物品,包括所需要的計算機軟件。其效用主要通過物理等方式獲得。
- 注冊與備案:這是兩種不同的市場準入方式。
- 注冊:適用于風險較高的第二類、第三類醫療器械。需要進行臨床試驗(部分情形可豁免)、技術審評、體系核查等嚴格審查,以獲得《醫療器械注冊證》。
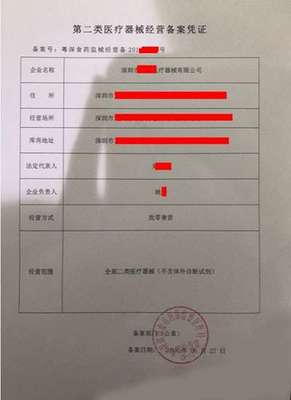
- 備案:適用于風險較低的第一類醫療器械。備案人只需提交備案資料,藥品監督管理部門對提交的資料進行形式審查,存檔備查,發放《第一類醫療器械備案憑證》。
醫護人員防護用品,如醫用防護口罩、醫用防護服、手術衣、隔離衣、無菌手套等,根據其預期用途和風險等級,絕大部分被劃分為第二類(如大多數外科口罩、手術衣)或第三類醫療器械(如用于高風險操作的醫用防護口罩、防護服)。因此,它們通常需要履行注冊程序,而非簡單的備案。
二、 進口醫療器械注冊備案全流程解析
以下流程以風險較高的第二、三類醫療器械注冊為主干,第一類備案流程相對簡化,包含在相應環節中。
第一階段:前期準備與產品判定(約1-3個月)
1. 指定中國代理人:境外申請人必須指定中國境內的企業法人作為其代理人,履行相關法律義務,如申請注冊、承擔連帶責任、協助召回等。
2. 產品分類判定:根據《醫療器械分類目錄》,明確申請產品的管理類別(Ⅰ、Ⅱ、Ⅲ類)。這是決定后續路徑的關鍵。
3. 檢測路徑規劃:確定產品是否需要在中國境內進行檢測,以及是否可利用境外臨床試驗數據或進行臨床試驗。
第二階段:檢測與臨床評價(時間差異巨大,數月到數年不等)
1. 產品檢測:通常需要在NMPA認可的境內醫療器械檢測機構進行全性能注冊檢驗,取得合格的檢測報告。這是注冊申報的基石。
2. 臨床評價:
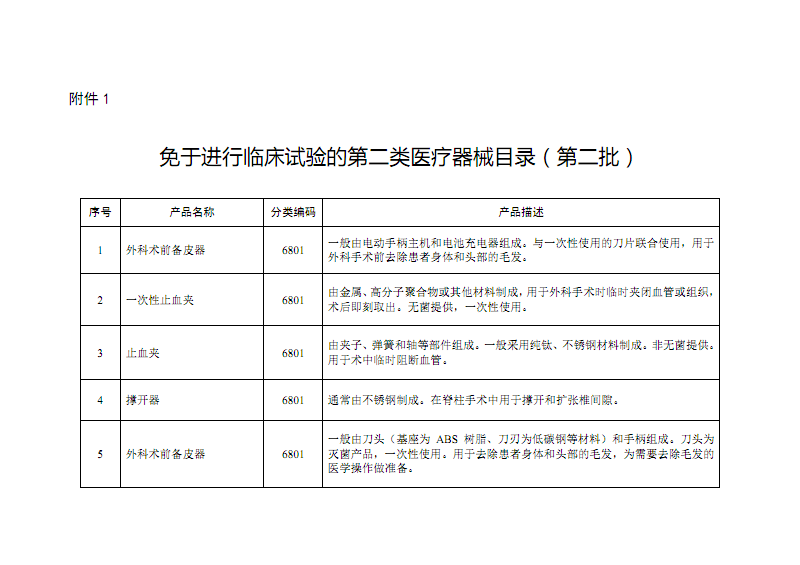
* 對于列入《免于臨床評價醫療器械目錄》的產品,可免于進行臨床評價。
- 其余產品需通過臨床試驗或同品種比對的路徑完成臨床評價。臨床試驗需在具備資質的醫院進行,并獲得倫理委員會批準,周期長、成本高。同品種比對需詳盡證明產品與已上市同類產品在安全有效性上等同。
第三階段:注冊申報與審評審批(Ⅱ類約1-2年,Ⅲ類約2-4年)
1. 體系核查:NMPA可能對境外生產場地進行質量管理體系現場核查,或委托當地監管機構核查。
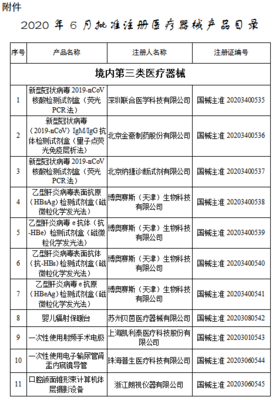
2. 提交注冊申請:通過NMPA醫療器械注冊電子申報系統(eRPS)提交全套技術資料,包括研究資料、檢測報告、臨床評價資料、生產制造信息、產品說明書和標簽樣稿等。
3. 技術審評:審評中心對資料進行科學審核,可能發出補充資料通知。此階段是核心,需要與審評機構密切溝通。
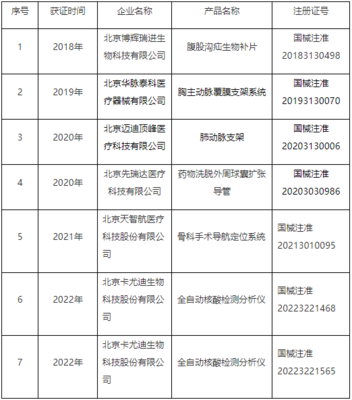
4. 行政審批與發證:技術審評通過后,進入行政審批環節,最終作出準予注冊或不予注冊的決定。準予注冊的,頒發《醫療器械注冊證》。
第四階段:備案(針對第一類醫療器械)
流程大幅簡化:準備備案資料(包括產品檢驗報告、說明書等)→ 通過eRPS系統提交 → 所在地省級藥監局形式審核 → 符合要求的,予以備案并公示,發放備案憑證。
三、 醫護人員防護用品注冊的特殊關注點
- 應急審批與優先通道:在公共衛生事件應急狀態下(如新冠疫情),對于急需的防護用品,NMPA設有應急審批程序,極大壓縮審評時間。但疫情常態化后,新產品的注冊仍需走標準流程。
- 標準符合性:產品必須符合強制性國家標準(GB)或行業標準(YY),例如GB 19083-2010《醫用防護口罩技術要求》、GB 19082-2009《醫用一次性防護服技術要求》。境外標準(如ASTM, EN)需進行比對,證明其等效性或更優性。
- 生物相容性與微生物指標:與皮膚、黏膜接觸的防護用品(如手套、口罩內層)需提供詳盡的生物相容性評價報告。無菌產品需嚴格驗證滅菌工藝和無菌保證水平。
- 標簽與說明書:必須具有完整的中文標簽和說明書,內容需符合中國法規要求,包括產品名稱、型號規格、生產企業信息、中國代理人信息、注冊證編號、生產日期、使用說明、禁忌癥等。
四、 常見挑戰與建議
- 挑戰:法規理解差異、臨床評價要求高、檢測周期長、審評溝通成本高、體系核查跨國協調難。
- 建議:
- 盡早介入:在產品研發早期即引入中國法規要求。
- 依靠專業伙伴:選擇經驗豐富、靠譜的中國代理人和國內法規咨詢服務團隊。
- 確保質量體系合規:確保境外生產質量體系符合中國《醫療器械生產質量管理規范》要求。
- 主動溝通:與檢測機構、審評中心保持積極、專業的溝通。
###
進口醫療器械及醫護人員防護用品的注冊備案是一個嚴謹、復雜且耗時的系統工程,涉及技術、法規和管理的深度融合。全面理解流程、充分準備資料、嚴格遵守法規,并與專業機構緊密合作,是成功獲得中國市場準入許可、保障產品合法合規銷售與使用的關鍵。隨著中國醫療器械法規的持續完善與國際接軌,這一過程正朝著更加科學、透明和高效的方向發展。
如若轉載,請注明出處:http://m.gd6888.cn/product/49.html
更新時間:2026-04-14 12:39:36